
Ниже приведены источники, использованные при составлении конспекта по теме «Гальваническое цинкование»
Технологический процесс цинкования электролизом заключается в следующем: стальные конструкции, подвергаемые цинкованию, и цинковые пластины погружаются в ванну с электролитом. Пластины и конструкции подключаются к источнику постоянного тока. Во время электролиза цинковый анод растворяется, и оседает на поверхности стального изделия.
…
Адгезия гальванических покрытий обеспечивается молекулярными силами при взаимодействии молекул цинка и основного металла. Так как, на силу этого взаимодействия влияет наличие любых пленок (жировых или окисных) на поверхности покрываемых изделий, чего не удается полностью избежать при массовом производстве, толщина гальванических покрытий обычно не превышает 20 - 30 мкм.
…
Недостатки: Электролитическое цинкование имеет серьёзный недостаток: необходима очистка сточных вод от цинка. Цена цинкового покрытия, получаемого этим методом, складывается не только из стоимости электролита и цинка. Электрохимическое цинкование сопровождается образованием экологически опасных отходов. Очистка сточных вод от ионов цинка достаточно дорогостоящая технология, требующая строительства очистных сооружений, потому иногда экономически более выгодно проводить цинкование метала, используя безэлектролитное цинкование.
Масса осажденного металла зависит не только от времени гальванической обработки и плотности тока, но и от вида покрытия и ванны. Эта зависимость выражается законом Фарадея, который является основой для расчетов, необходимых в каждодневной практике:
m=kIt,
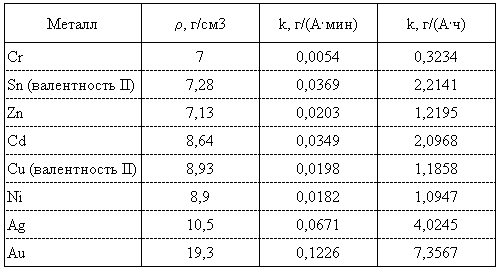
где m – масса вещества, осажденного на катоде, г; I – сила протекающего через электролит тока, А; t – длительность протекания тока, ч; k – электрохимический эквивалент или масса вещества (в граммах), осажденного в течение 1 ч при силе тока 1 А. В табл. 1 приведены электрохимические эквиваленты для металлов, наиболее часто применяемых в гальванотехнике.
…
Выход по току
Немногие электрохимические процессы идут точно в соответствии с законом Фарадея, так как часть тока может быть израсходована на побочные процессы, например, на выделение водорода.
Отношение массы осажденного на катоде металла к теоретической массе, следующей из закона Фарадея, называется катодным выходом по току и приводится в процентах.
Выход по току зависит от состава электролита и параметров осаждения.
…
В практической гальванотехнике закон Фарадея, имеет, следовательно, более развернутый вид, учитывающий катодный выход по току, h %;
m=kIth.
Пути улучшения распределения материала на поверхности катода
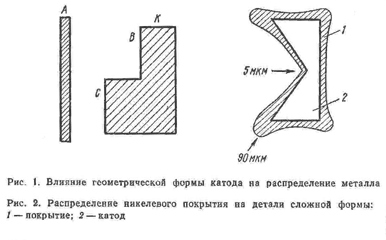
Толщина электролитически осажденного металлического покрытия (особенно на изделиях сложной формы) не одинакова. Одна из причин этого – геометрическая форма катода (рис. 1). Напротив плоского анода А находится катод К сложной формы. Расстояние от анода до плоскости В вдвое больше расстояния до плоскости С, и казалось бы на поверхности С должно осадиться металла в два раза больше, чем на плоскости В. В действительности дело обстоит гораздо сложнее, так как кроме геометрических факторов проявляется действие поляризации – сложного электрохимического явления.
…
В некоторых ваннах, например, хромовых получают покрытия с большой разнотолщинностью, в других, например, для щелочного лужения, цианидного меднения – с меньшей. В первом случае говорим, что ванна имеет небольшую кроющую способность, а во втором – большую.
…
Даже в ваннах с хорошей кроющей способностью покрытие осаждается неравномерно. На ребрах и выпуклых местах толщина больше, чем в углублениях. На рис. 2 представлено распределение никелевого покрытия на поверхности детали сложной формы, подвергнутой никелированию в нормальных производственных условиях. На выпуклых поверхностях покрытие достигает толщины 90 мкм, а в углублениях только 5 мкм (форма покрытия показана на заштрихованных участках).
…
Наибольшее утолщение покрытия обычно наблюдается на острых краях. Во избежание этого возле ребер размещают вспомогательные металлические катоды, соединенные с покрываемой деталью.
…
Применение вспомогательных катодов и экранов довольно затруднительно и должно рассматриваться как крайняя мера. Во многих случаях достаточно умело расположить детали на подвесках.
…
Механизм защитного действия цинковых покрытий на стали представлен в упрощенном виде на рис. 7, где показано в увеличенном виде поперечное сечение стального образца, покрытого электролитическим слоем цинка. Если в неплотностях покрытия, вызванных пористостью или механическим повреждением, накопится влага, то образуется коррозионная пара, в которой цинк является растворимым анодом, а сталь - катодом. В результате этого наступает разрушение самого покрытия, а сталь остается нетронутой. Покрытие защищает стальную подложку до полного разрушения цинка. Следовательно, толщина должна быть выбрана соответственно эксплуатационным условиям. Покрытия этого типа называются анодными.